De ce a fost adus vaccinul HEXAXIM în România
• Ȋn 2014, 15 județe au raportat 20 de cazuri cu reacții adverse după vaccinarea cu HEXACIMA • La 30 decembrie 2015 Agenția Națională a Medicamentului a acordat pentru HEXAXIM, un vaccin similar, destinat exclusiv piețelor din afara Uniunii Europene, „autorizația pentru furnizarea de medicamente pentru nevoi speciale” • Agenția Europeană pentru Medicamente avertizase că e nevoie de studii suplimentare pentru HEXAXIM • Sanofi Pasteur s-a angajat să le efectueze, iar vaccinul a fost adus în România.
Ȋn 2012, 38 de județe au raportat 197 de cazuri cu reacții adverse la BCG SSI, un vaccin fabricat de Statens Serum Institut din Danemarca. Un copil a murit. Raed Arafat a sistat vaccinarea, însă după numai opt zile a dat ordin ca ea să fie reluată, la indicațiile experților Organizației Mondiale a Sănătății și ai Centrului European de Prevenire și Control a Bolilor Transmisibile, veniți special în România. Anul următor, în 2013, 58 de copii au prezentat reacții adverse după ce au fost vaccinați cu BCG SSI. Cazurile au fost raportate din numai 29 de județe. După 7 luni de la vaccinarea BCG, un alt copil a fost diagnosticat cu tuberculoză.
Ȋn 2014, Ministerul Sănătății a achiziționat doar vaccinul BCG produs de BB-NCIPD Ltd. Bulgaria și distribuit de Intervax Canada. Ȋn anii anteriori se înregistraseră reacții adverse și după administrarea acestui vaccin (2012 – două cazuri de RAPI, 2013 – o limfadenopatie supurată), însă ele nu fuseseră atât de multe și de grave ca în cazul vaccinului produs în Danemarca.
Ȋn 2014, doar 15 județe au raportat cazurile de reacții adverse, din totalul celor 42. București lipsește din listă. Analiza realizată de CNCSBT în baza acestor informații incomplete este, prin urmare, irelevantă la nivel național. Au fost înregistrate doar 28 de cazuri de RAPI, din care 27 confirmate.
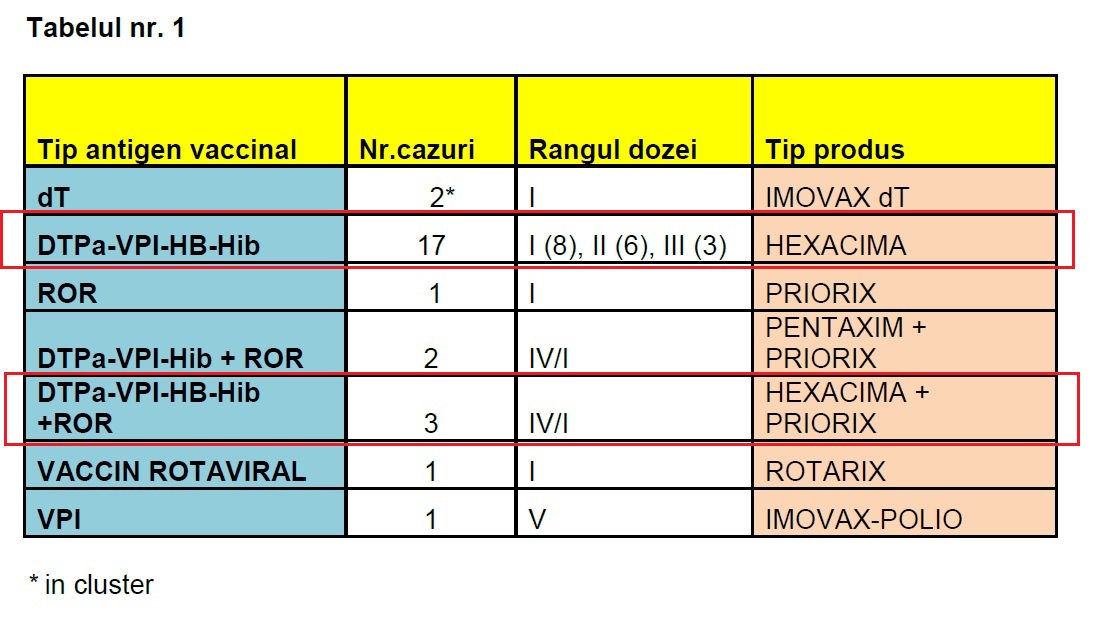
Și, deși oficial nu ni se dezvăluie decât vârful aisbergului, concluziile sunt îngrijorătoare: 20 din cele 28 de cazuri înregistrate în 2014 sunt reacții adverse apărute după administrarea unui vaccin nou introdus pe piața românească: HEXACIMA, produs de Sanofi Pasteur SA din Franța. Ȋn prospectul vaccinului(disponibil, AICI), care fusese autorizat cu doar câteva luni în urmă, în aprilie 2013, scrie: „Acest medicament face obiectul unei monitorizări suplimentare. Acest lucru va permite identificarea rapidă de noi informații referitoare la siguranță. Profesioniștii din domeniul sănătății sunt rugați să raporteze orice reacții adverse suspectate”.
Ȋn România anului 2014, doar în 15 DSP-uri mai existau câțiva profesioniști... „Frisonete, tegumente și mucoase palide, cu tentă cianotică, reactivitate foarte scazută”, au raportat ei ca RAPI pentru HEXACIMA. „La aproximativ 5 minute după administrare: somnolență, paloare, hipotonie, areactivitate la stimului externi.” „La 2,5 ore după vaccinare – criză de hipotonie generalizată, cu reversia globilor oculari, paloare, cu durata de 2-3 minute; crize de plâns și agitație.” „Febră, convulsie hipotonă în context febril, cu plafonarea privirii, cu durata de 4 - 5 minute.”
Nu știm încă ce și câte efecte adverse a provocat vaccinul HEXACIMA și în 2015. Deși suntem în luna martie, analiza CNCSBT a cazurilor de RAPI înregistrate anul trecut întârzie să apară.
Cert este că la 9 februarie a.c., Casa Națională de Asigurări de Sănătate trimitea în teritoriu o informare potrivit căreia HEXACIMA era înlocuit cu omologul HEXAXIM, produs tot de Sanofi Pasteur SA (Franța) și distribuit în România de firma Polisano S.R.L.. Ce știm despre acest vaccin? Știm că el nu figurează în baza de date a Agenției Europene pentru Medicamente.
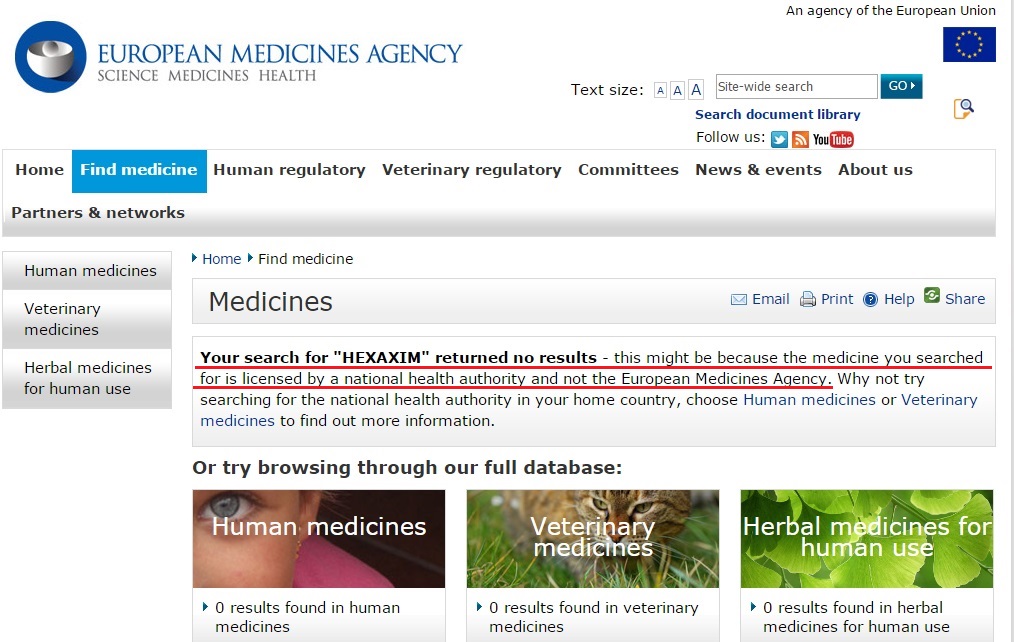
Ȋn iunie 2012, Agenția Europeană a Medicamentului (EMA) a emis însă un aviz (disponibil AICI) prin care stabilește că „beneficiile vaccinului HEXAXIM sunt mai mari decât riscurile sale” și că „acesta poate fi utilizat în regiunile din afara Uniunii Europene”. Era primul aviz de acest tip eliberat pentru un vaccin.
„Medicamentul Hexaxim 0,5 ml suspensie injectabilă este destinat exclusiv piețelor din afara Uniunii Europene”, avertiza EMA.
Ȋntr-un comunicat emis în martie 2015 și publicat în decembrie 2015, Agenția Europeană a Medicamentului subliniază că avizul pentru avizul HEXAXIM a fost acordat de Comitetul pentru Medicamente de Uz Uman (CHMP) „în cadrul cooperării EMA cu Organizația Mondială a Sănătății, prin care CHMP furnizează avize cu privire la medicamentele care nu sunt destinate utilizării în UE, dar care sunt necesare pentru prevenirea sau tratarea bolilor.” Ȋn același comunicat, se precizează și că „CHMP a remarcat că este nevoie de mai multe informații cu privire la efectele Hexaxim la copiii cu un sistem imunitar slăbit, dar și atunci când el este utilizat în asociere cu alte vaccinuri. Compania (n.r. - Sanofi Pasteur Franța) s-a angajat să efectueze studii suplimentare.”

La scurt timp, HEXAXIM a fost adus în România, unde Agenția Națională a Medicamentului și a Dispozitivelor Medicale (ANMDM) a acordat Autorizația pentru furnizarea de medicamente pentru nevoi speciale nr. 185/30.12.2015. Pe site-ul ANMDM nu sunt disponibile nici „Rezumatul Carateristicilor Produsului”, nici „Prospectul” și nici „Ambalajul”( vezi AICI).
Conform informării remise de distribuitorul HEXAXIM, SC Polisano SRL, din faxul trimis medicilor prin CNAS, ANMDM a aprobat distribuirea în România vaccinului HEXAXIM, „ca urmare a problemelor temporare de aprovizionare cu vaccinul HEXACIMA”.
Sanofi Pasteur obținuse, la 9 ianuarie 2014, autorizația de distribuire a vaccinului HEXAXIM în Kazahstan. O parte din dozele destinate acelei piețe au fost reorientate spre România. Ȋntr-un ambalaj și cu un prospect scrise în alfabet chirilic. Abia la 24 februarie medicii au primit informațiile și în limba română( disponibile, AICI).
Din atenționările pe care le făcea Agenția Europeană a Medicamentului, în prospectul tradus în limba română au rămas frazele: „Nu sunt disponibile date privind sugarii născuți prematur. Totuși, poate fi observat un răspuns imun mai redus, iar nivelul de protecție clinică nu este cunoscut”. „În cazul în care se ia în considerare administrarea concomitentă a vaccinului Hexaxim cu un alt vaccin, imunizarea trebuie efectuată la nivelul unor locuri diferite de injectare.” Dar și „Vaccinului Hexaxim (sic!) nu trebuie amestecat cu niciun alt vaccin sau cu alte medicamente administrate parenteral (n.r. - pe altă cale decât pe cea digestivă).”
Și HEXAXIM, ca și HEXACIMA, e un medicament ce „face obiectul unei monitorizări suplimentare. Acest lucru va permite identificarea rapidă de noi informații referitoare la siguranță. Profesioniștii din domeniul sănătății sunt rugați să raporteze orice reacții adverse suspectate”.
La sfârșitul anului 2016, 10 județe din cele 42 vor trimite către centru „X” cazuri de RAPI, din care vor fi confirmate „X-Y”. Ȋn baza lor, CNCSBT va întocmi o analiză la nivel național în care, inevitabil, se va concluziona că „totul este bine”. Pentru copiii vaccinați, pentru părinții lor, pentru medicii responsabili, pentru producătorul vaccinului și pentru firma care-l distribuie. Firește, pentru copiii „X-Y” nu va mai fi bine, dar asta-i jocul vaccinului, de-a „An tan te, dize mane pe”... Și nu toți părinții știu regulile jocului.
Ȋn prezentarea oricărui vaccin se pune accentul pe balanța beneficii/riscuri. Firește, cadrele medicale au datoria să apese doar pe un taler al balanței. Ȋnsă părintele este cel care cântărește și ia decizia finală în privința vaccinării copilului său. Și cred că părintele trebuie să fie în cunoștință de cauză, atunci când ia această decizie. Pentru că nu optează pentru vreun tip de credit la bancă sau pentru vreo vacanță all inclusive, ci ia o decizie majoră, ce poate afecta viața și sănătatea copilului său. Și trebuie să aibă acces la TOATE informațiile!
Pentru ca oamenii să fie corect informați, medicii ar trebui să-și facă datoria și să raporteze cazurile de RAPI. Direcțiile de Sănătate Publică ar trebui să-și facă datoria și să transmită datele către Centrul Național de Supraveghere și Control al Bolilor Transmisibile. CNSCBR ar trebui să-și facă datoria și să ceară aceste informări DSP-urilor, nu doar să constante, senin și periodic, lipsa lor. Ministerul Sănătății ar trebui să-și facă datoria și să verifice modul în care funcționează sistemul de supraveghere a reacțiilor adverse post-vaccinale.
Iar noi, la rându-ne, ar trebui să ne facem datoria și să cerem public salvarea Institutului Cantacuzino și reluarea producției de vaccinuri românești. Pentru că doar așa vom fi cu adevărat siguri de ceea ce scrie în prospect. Sau pe ambalaj. Și nu ne vom trezi că medicul ne înțeapă copilul spunând că-l vaccinează cu HEXAXIM-ul scos dintr-o cutie pe care scrie, în limba rusă, „GHECSACSIM”...
(N.a. - Informații oficiale (incomplete) despre Reacțiile Adverse Post-vaccinale Indezirabile (RAPI) sunt disponibile pe site-ul: http://www.cnscbt.ro/index.php/analiza-date-supraveghere/rapi-1)
Donează pentru ActiveNews!
ActiveNews nu a primit niciodată altă publicitate decât cea automată, de tip Google, din care o îndepărtăm pe cea imorală. Aceasta însă nu ne asigură toate costurile.
Ziarele incomode sunt sabotate de Sistem. Presa din România primeste publicitate (adică BANI) doar în măsura în care este parte a Sistemului sau/și a Rețelei Soros. Sau dacă se supune, TACE sau MINTE.
ActiveNews NU vrea să se supună. ActiveNews NU vrea să tacă. ActiveNews NU vrea să mintă. ActiveNews VREA să rămână exclusiv în slujba Adevărului și a cititorilor.
De aceea, are nevoie de cititorii săi pentru a supraviețui așa cum este acum. Dacă și tu crezi în ceea ce credem noi, te rugăm să ne sprijini să luptăm în continuare pentru Adevăr, pentru România!
ActiveNews nu a primit niciodată altă publicitate decât cea automată, de tip Google, din care o îndepărtăm pe cea imorală. Aceasta însă nu ne asigură toate costurile.
Ziarele incomode sunt sabotate de Sistem. Presa din România primeste publicitate (adică BANI) doar în măsura în care este parte a Sistemului sau/și a Rețelei Soros. Sau dacă se supune, TACE sau MINTE.
ActiveNews NU vrea să se supună. ActiveNews NU vrea să tacă. ActiveNews NU vrea să mintă. ActiveNews VREA să rămână exclusiv în slujba Adevărului și a cititorilor.
De aceea, are nevoie de cititorii săi pentru a supraviețui așa cum este acum. Dacă și tu crezi în ceea ce credem noi, te rugăm să ne sprijini să luptăm în continuare pentru Adevăr, pentru România!
RO02BTRLRONCRT0563030301 (lei) | RO49BTRLEURCRT0563030301 (euro)
Pe același subiect

De la ”Vaccinare în viteza a șasea”, la Terapie Intensivă. Mihai Leu, în stare critică la Spitalul Fundeni din București. Fostul campion la box și raliuri a fost transportat de urgență cu elicopterul

Robert F. Kennedy: ”Gardasil este probabil cel mai rău vaccin în masă pe care l-am văzut vreodată”

Celebra actriță Teddi Mellencamp este în fază terminală de cancer generalizat, la 43 de ani, după ce s-a vaccinat Covid în 2021

Colegiul Pseudo-Medicilor reîncepe prigonirea Medicului Răzvan Constantinescu după ce acesta a ridicat problema MORȚILOR SUBITE din rândul cadrelor medicale în urma vaccinării cu seruri experimentale Covid. ”Abia aștept să-i umilesc din nou!”

Mort subit după vaccin, în floarea vieții - a debutat post-mortem...

Slovacia lansează o anchetă privind vaccinul Covid-19 după constatările de contaminare cu ADN
Recomandările noastre

22 aprilie 1990, startul Pieței Universității. În urmă cu 35 de ani începea cea mai amplă manifestație anticomunistă din Europa Centrală și de Est. VIDEO și GALERIE FOTO

Alex Jones și Tucker Carlson despre Lupta pentru Adevăr: Globalism, Trump, Israel, Planuri Secrete pentru Al Treilea Război Mondial, WEF, CIA, 9/11 - O EMISIUNE-BOMBĂ tradusă în română - VIDEO
Secțiuni: Sănătate
Subiecte: Vaccinarea obligatorie Vaccinuri periculoase
Organizații: Ministerul Sănătății
Tip conținut: Știri

 Ministerul Sănătăţii despre proiectul legii privind vaccinarea: Statul ar putea să îşi asume complicaţiile sau sechelele apărute în urma VACCINĂRII
Ministerul Sănătăţii despre proiectul legii privind vaccinarea: Statul ar putea să îşi asume complicaţiile sau sechelele apărute în urma VACCINĂRII 

Autentifică-te sau înregistrează-te pentru a trimite comentarii.
Comentarii (3)